علت پیری در ترکیبی از عوامل ژنتیکی، اپیژنتیکی و محیطی نهفته است. در حالی که برخی از افراد با سرعت بیشتری علائم پیری را تجربه میکنند، دیگران بهطور طبیعی روند پیری کندتری دارند. مطالعات نشان دادهاند که ژنهایی مانند FOXO3، SIRT1 و KLOTHO نقش مهمی در افزایش طول عمر و مقاومت در برابر استرسهای سلولی دارند. از سوی دیگر، جهشهای مضر در ژنهایی مانند BRCA1/2 میتوانند روند پیری را تسریع کنند.
علاوه بر این، ابزارهایی مانند ساعت اپیژنتیک Horvath Clock به ما امکان میدهند تا سن بیولوژیکی خود را با دقت بیشتری اندازهگیری کنیم و اقدامات پیشگیرانهای برای کاهش سرعت پیری انجام دهیم. در این مقاله، به بررسی دقیقتر نقش ژنتیک در پیری، ابزارهای سنجش سن بیولوژیکی و راهکارهای علمی برای مقابله با پیری زودرس میپردازیم.
نقش ژنها در کُند یا سریع شدن روند پیری
علت پیری در تعامل پیچیدهای از عوامل ژنتیکی، اپیژنتیکی و محیطی نهفته است. ژنها با تأثیر بر فرآیندهای سلولی مانند ترمیم DNA، مقاومت در برابر استرس اکسیداتیو و تنظیم متابولیسم، نقش مهمی در تعیین سرعت پیری دارند. برخی ژنها مانند FOXO3، SIRT1 و KLOTHO با افزایش طول عمر مرتبط هستند، در حالی که جهشهای مضر در ژنهایی مانند BRCA1/2 و WRN میتوانند منجر به پیری زودرس شوند. درک این ژنها و تأثیر آنها بر روند پیری میتواند به توسعه راهکارهای مؤثر برای مقابله با پیری زودرس کمک کند.
ژنهای طول عمر؛ چه ژنهایی به افزایش عمر کمک میکنند؟
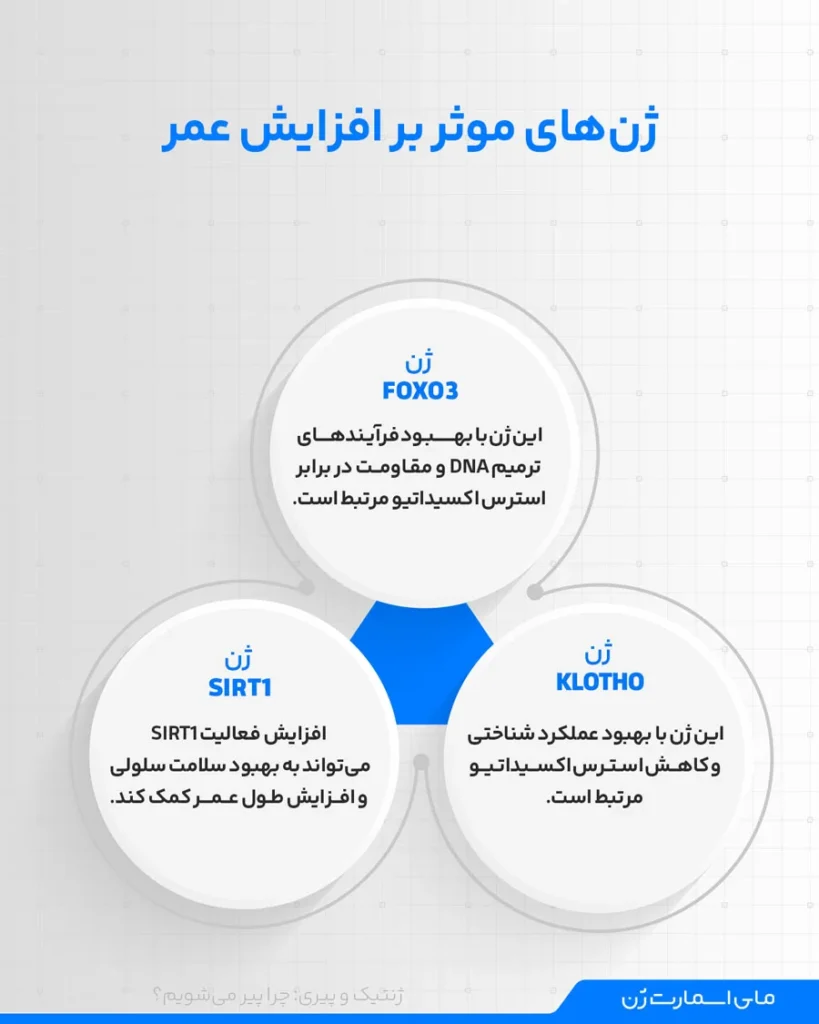
دلیل پیری زودرس در مردان و زنان به ژنهای طول عمر بستگی دارد. پیری زودرس زمانی رخ میدهد که عوامل محیطی، «ژنهای طول عمر» را خاموش کنند. با بهرهگیری از دانش بیوهکینگ و طول عمر، میتوان از طریق اصلاح تغذیه و تمرینات تخصصی، این ژنها (مانند SIRT1) را فعال کرد و روند فرسودگی سلولی را به تأخیر انداخت. ژنهای مرتبط با پیری:
- FOXO3: تحقیقات انجامشده در هاوایی نشان دادهاند که افراد دارای واریانتهای خاصی از این ژن، ۲.۷ برابر بیشتر احتمال دارد که به سن ۹۵ سالگی برسند. این ژن با بهبود فرآیندهای ترمیم DNA و مقاومت در برابر استرس اکسیداتیو مرتبط است.
- SIRT1: این ژن با تنظیم فرآیندهای متابولیکی و ترمیم DNA نقش مهمی در کند کردن روند پیری دارد. مطالعات نشان دادهاند که افزایش فعالیت SIRT1 میتواند به بهبود سلامت سلولی و افزایش طول عمر کمک کند.
- KLOTHO: تحقیقات بر روی موشها نشان دادهاند که افزایش بیان این ژن میتواند طول عمر را تا ۳۰٪ افزایش دهد. این ژن با بهبود عملکرد شناختی و کاهش استرس اکسیداتیو مرتبط است.
کدام تغییرات ژنتیکی روند پیری را سرعت میبخشند؟
برخی جهشهای ژنتیکی میتوانند منجر به پیری زودرس و افزایش خطر ابتلا به بیماریهای مرتبط با سن شوند:
- BRCA1/2: جهش در این ژنها با افزایش خطر ابتلا به سرطانهای پستان و تخمدان مرتبط است. همچنین، این جهشها میتوانند منجر به کاهش ذخیره تخمدانی در زنان شوند. این موضوع در دلیل پیری زودرس در زنان نیز مورد بحث قرار گرفته است.
در کنار عوامل ژنتیکی مانند جهش در ژنهای BRCA1 و BRCA2، سبک زندگی و الگوی تغذیه نیز در سلامت تخمدان و پیشگیری از پیری زودرس نقش قابلتوجهی دارند. رژیمهای غذایی سرشار از آنتیاکسیدان، فیبر و چربیهای سالم میتوانند از سلولهای تخمدان در برابر استرس اکسیداتیو محافظت کنند و تعادل هورمونی را بهبود دهند.
در مقابل، رژیمهای پرقند یا دارای شاخص گلیسمی بالا ممکن است روند التهاب و مقاومت به انسولین را تشدید کنند. برای آشنایی با تأثیر تغذیه بر عملکرد تخمدان و انتخاب برنامه غذایی مناسب، پیشنهاد میکنیم مقالهٔ رژیم غذایی برای تخمدان پلی کیستیک را بخوانید.
- WRN: جهش در این ژن منجر به سندرم ورنر میشود که با پیری زودرس، کاهش طول عمر و افزایش خطر ابتلا به سرطانها همراه است.

مای اسمارت ژن با ارائه چکاپهای تخصصی در حوزههای سلامت (شناسایی ریسکهای ژنتیکی بیماریها) نیاکان (شجره نامه ژنتیکی) تغذیه (نیازهای ضروری بدن و رژیم ژنتیک) شناختی (بررسی پتانسیلهای ذاتی و صفات روانشناختی برای توسعه فردی ) به شما کمک میکند تا تصمیماتی آگاهانه برای زندگیتان بگیرید. همین امروز مشاوره بگیرید.
برای دریافت مشاوره رایگان در زمینه تست های ژنتیکی متفاوت اطلاعات زیر را تکمیل کنید.
آیا میتوان سن بیولوژیکی را تغییر داد؟

ساعتهای اپیژنتیک ابزارهایی هستند که با اندازهگیری الگوهای متیلاسیون DNA، سن بیولوژیکی فرد را تعیین میکنند. مطالعات نشان دادهاند که این ساعتها میتوانند پیشبینی دقیقی از طول عمر و خطر ابتلا به بیماریهای مرتبط با پیری ارائه دهند. برای مثال، ساعت اپیژنتیک Horvath Clock با دقت بالایی میتواند سن بیولوژیکی را اندازهگیری کند.
تفاوت سن کرونولوژیک و سن بیولوژیک چیست؟
- سن کرونولوژیک: تعداد سالهایی است که از تولد فرد گذشته است.
- سن بیولوژیک: نشاندهنده وضعیت فیزیولوژیکی بدن است و میتواند تحت تأثیر عوامل ژنتیکی، سبک زندگی و محیط قرار گیرد.
برای مثال، فردی ممکن است ۵۰ سال سن کرونولوژیک داشته باشد، اما به دلیل سبک زندگی سالم، سن بیولوژیکی او ۴۵ سال باشد.
تستهای اپیژنتیک؛ چگونه سن واقعی بدن را بسنجیم؟
تستهای اپیژنتیک با اندازهگیری الگوهای متیلاسیون DNA، سن بیولوژیکی فرد را تعیین میکنند. برای مثال، تست myDNAge با استفاده از ساعت اپیژنتیک Horvath Clock، سن بیولوژیکی را با دقت بالایی اندازهگیری میکند. این اطلاعات میتوانند به فرد کمک کنند تا با اتخاذ سبک زندگی سالم، روند پیری را کندتر کند.
آزمایشهای کلیدی برای سنجش روند پیری

در بحث دلیل پیری زودرس در مردان و زنان و برای ارزیابی دقیقتر وضعیت بیولوژیکی بدن و پیشبینی روند پیری، میتوان از آزمایشهای زیر استفاده کرد:
| نام آزمایش | هدف | روش اندازهگیری | تفسیر نتایج |
| طول تلومر | ارزیابی سلامت سلولی و پیشبینی طول عمر | qPCR، FISH | تلومرهای کوتاهتر با پیری زودرس و بیماریهای مرتبط با سن مرتبط هستند. |
| ساعت اپیژنتیک (Horvath, GrimAge) | تعیین سن بیولوژیکی بر اساس الگوهای متیلاسیون DNA | آنالیز متیلاسیون DNA در سایتهای CpG خاص | اختلاف بین سن بیولوژیکی و کرونولوژیکی میتواند نشاندهنده سرعت پیری باشد. |
| سطح IGF-1 | بررسی مسیرهای رشد و متابولیسم مرتبط با پیری | آزمایش خون | سطوح بالا ممکن است با افزایش خطر سرطان و پیری زودرس مرتبط باشند. |
| فعالیت mTOR و AMPK | ارزیابی تعادل بین رشد سلولی و حفظ سلامت سلولی | بررسی بیان ژنها و پروتئینهای مرتبط در نمونههای بافتی | فعالیت بیش از حد mTOR با پیری زودرس و بیماریهای مزمن مرتبط است؛ AMPK نقش محافظتی دارد. |
| تستهای ترکیبی نشانگرهای زیستی | ارزیابی جامع سلامت بیولوژیکی و پیشبینی خطر بیماریهای مرتبط با سن | ترکیب دادههای فیزیولوژیکی و ژنومی | ارائه نمای کلی از وضعیت سلامت و پیشبینی روند پیری. |
مطالعات نشان دادهاند که ترکیب این آزمایشها میتواند تصویر دقیقتری از وضعیت بیولوژیکی فرد ارائه دهد و به اتخاذ تصمیمات بهداشتی مؤثرتر کمک کند.
مطلب پیشنهادی: با افزایش سن، توانایی بدن در جذب و استفاده از پروتئین کاهش مییابد، به همین دلیل آشنایی با راههای جذب پروتئین اهمیت بیشتری پیدا میکند.
تلومرها و پیری؛ پایان خط زندگی سلولها کجاست؟
علت پیری در سطح سلولی به کوتاه شدن تدریجی تلومرها، ساختارهای حفاظتی در انتهای کروموزومها، مرتبط است. با هر تقسیم سلولی، تلومرها کوتاهتر میشوند و زمانی که به حد بحرانی میرسند، سلول وارد فاز پیری یا مرگ میشود. مطالعات نشان دادهاند که طول تلومر با طول عمر و بروز بیماریهای مرتبط با سن ارتباط مستقیم دارد.
تلومراز؛ آنزیمی برای جاودانگی؟
تلومراز آنزیمی است که میتواند طول تلومرها را حفظ یا افزایش دهد. در سلولهای بنیادی و برخی سلولهای سرطانی، فعالیت تلومراز بالا است. تحقیقات نشان دادهاند که افزایش فعالیت تلومراز در سلولهای انسانی میتواند عمر آنها را افزایش دهد، اما خطر بروز سرطان نیز افزایش مییابد.
کوتاه شدن تلومر؛ ارتباط آن با استرس، تغذیه و سبک زندگی
مطالعات متعدد نشان دادهاند که عوامل سبک زندگی مانند استرس مزمن، تغذیه نامناسب، کمخوابی و عدم فعالیت بدنی میتوانند منجر به کوتاه شدن سریعتر تلومرها شوند. برای مثال در مورد دلیل پیری زودرس در زنان، تحقیقی در دانشگاه کالیفرنیا نشان داد که زنان یائسهای که استرس بیشتری را تجربه میکردند، تلومرهای کوتاهتری داشتند.
مسیرهای سلولی تنظیمکننده پیری

علت پیری در سطح مولکولی به مسیرهای سیگنالینگ سلولی مانند IGF-1/Insulin، mTOR و AMPK مرتبط است. این مسیرها نقش حیاتی در تنظیم رشد سلولی، متابولیسم و پاسخ به استرس دارند. تغییر در فعالیت این مسیرها میتواند بر سرعت پیری و بروز بیماریهای مرتبط با سن تأثیر بگذارد.
آیا کاهش کالری واقعا طول عمر را افزایش میدهد؟
تحقیقات نشان دادهاند که محدودیت کالری میتواند سطح IGF-1 را کاهش داده و فعالیت مسیر mTOR را مهار کند، که این امر با افزایش طول عمر در مدلهای حیوانی مرتبط است. برای مثال، مطالعهای در سال ۲۰۲۳ نشان داد که کاهش مصرف کالری منجر به کاهش سطح انسولین و IGF-1 و در نتیجه افزایش طول عمر در موشها شد.
تعادل بین رشد و حفظ سلامت سلولی
mTOR و AMPK دو مسیر سیگنالینگ کلیدی هستند که تعادل بین رشد سلولی و حفظ سلامت سلولی را تنظیم میکنند. فعالیت بیش از حد mTOR با پیری زودرس و بیماریهای مزمن مرتبط است، در حالی که فعالسازی AMPK میتواند فرآیندهای محافظتی مانند اتوفاژی را تحریک کرده و به افزایش طول عمر کمک کند.
چرا تولید انرژی سلولی با سن کاهش مییابد؟
میتوکندریها بهعنوان نیروگاههای سلولی، نقش حیاتی در تولید ATP دارند. با افزایش سن، عملکرد میتوکندریها کاهش مییابد که یکی از علتهای پیری محسوب میشود. مطالعات نشان دادهاند که کاهش جذب کلسیم توسط میتوکندریها در سنین بالا، منجر به اختلال در تولید انرژی و افزایش استرس اکسیداتیو میشود .
جهشهای میتوکندریایی؛ عامل پنهان پیری بافتی
جهشهای تجمعی در DNA میتوکندری (mtDNA) با افزایش سن، عملکرد میتوکندری را مختل کرده و به پیری زودرس در بافتها منجر میشوند. مطالعهای در eLife نشان داد که این جهشها در بافتهای مختلف بدن افزایش مییابند و با اختلالات متابولیکی و بیماریهای مرتبط با پیری مرتبط هستند .
آنتیاکسیدانها و CoQ10؛ چقدر مؤثرند؟
CoQ10 بهعنوان یک آنتیاکسیدان قوی، نقش مهمی در حفظ سلامت میتوکندریها دارد. مطالعات نشان دادهاند که مصرف CoQ10 میتواند استرس اکسیداتیو را کاهش داده و عملکرد میتوکندری را بهبود بخشد . با این حال، اثربخشی آن در بهبود طول عمر انسان هنوز نیاز به تحقیقات بیشتری دارد.
ارتباط ژنها با بیماریهای مرتبط با پیری؛ از آلزایمر تا دیابت
برخی از ژنها نقش مهمی در بروز بیماریهای مرتبط با پیری دارند. برای مثال، ژنهای مرتبط با دیابت نوع ۲ میتوانند خطر ابتلا به آلزایمر را افزایش دهند . همچنین، جهش در ژنهای خاص میتواند به اختلال در عملکرد میتوکندری و افزایش علت پیری زودرس منجر شود.

بیشتر بخوانید: نشانههای فراموشی در جوانی
راهکارهای علمی برای مقابله با پیری ژنتیکی
در مجموع، ترکیبی از سبک زندگی سالم، مصرف مکملهای مناسب و پیشرفتهای علمی در زمینه ژنتیک میتواند به کاهش پیری زودرس و افزایش کیفیت زندگی در سنین بالا کمک کند. در ادامه با این موارد بیشتر آشنا میشویم.
مطالعات نشان دادهاند که تغییرات در سبک زندگی میتوانند تأثیرات مثبتی بر ژنتیک پیری داشته باشند. برای مثال، مطالعهای در دانشگاه آکسفورد نشان داد که عوامل محیطی و سبک زندگی تأثیر بیشتری بر پیری دارند تا عوامل ژنتیکی . این شامل رژیم غذایی سالم، ورزش منظم و کاهش استرس است.
مداخلات دارویی و ژندرمانی
تحقیقات جدید در زمینه ژندرمانی نشان دادهاند که میتوان با استفاده از تکنیکهای خاص، روند پیری را معکوس کرد. برای مثال، درمان ژنی با استفاده از ژن Klotho در موشها باعث افزایش ۲۰٪ در طول عمر آنها شد . این نشان میدهد که مداخلات ژنتیکی میتوانند راهکارهای مؤثری برای مقابله با علت پیری زودرس باشند.
جمع بندی
علت پیری را میتوان در تعامل پیچیدهای از عوامل ژنتیکی، اپیژنتیکی و محیطی جستجو کرد. با پیشرفتهای علمی، اکنون میتوانیم با استفاده از ابزارهایی مانند ساعتهای اپیژنتیک و آزمایشهای ژنتیکی، سن بیولوژیکی خود را با دقت بیشتری اندازهگیری کنیم. این اطلاعات به ما امکان میدهند تا با اتخاذ سبک زندگی سالم، تغذیه مناسب و مدیریت استرس، روند پیری را کندتر کنیم.
علاوه بر این، تحقیقات نشان دادهاند که برخی از ژنها نقش مهمی در افزایش طول عمر دارند، در حالی که جهشهای مضر میتوانند روند پیری را تسریع کنند. با درک بهتر از این فرآیندها، میتوانیم اقدامات مؤثرتری برای حفظ سلامت و افزایش کیفیت زندگی در دوران پیری انجام دهیم.
منابع:
https://www.sciencedirect.com/science/article
https://journals.plos.org/plosgenetics
https://www.mayoclinic.org/healthy-lifestyle/healthy-aging/in-depth/aging/art-20046070
https://neurosciencenews.com/diet-lifestyle-biological-aging